Typer av hydrokarboner. Klassifikasjonene for hydrokarboner definert av IUPAC nomenclature of organic chemistry. Noen hydrokarboner danner polymerer slik som plasttypene polyetylen og polypropylen.
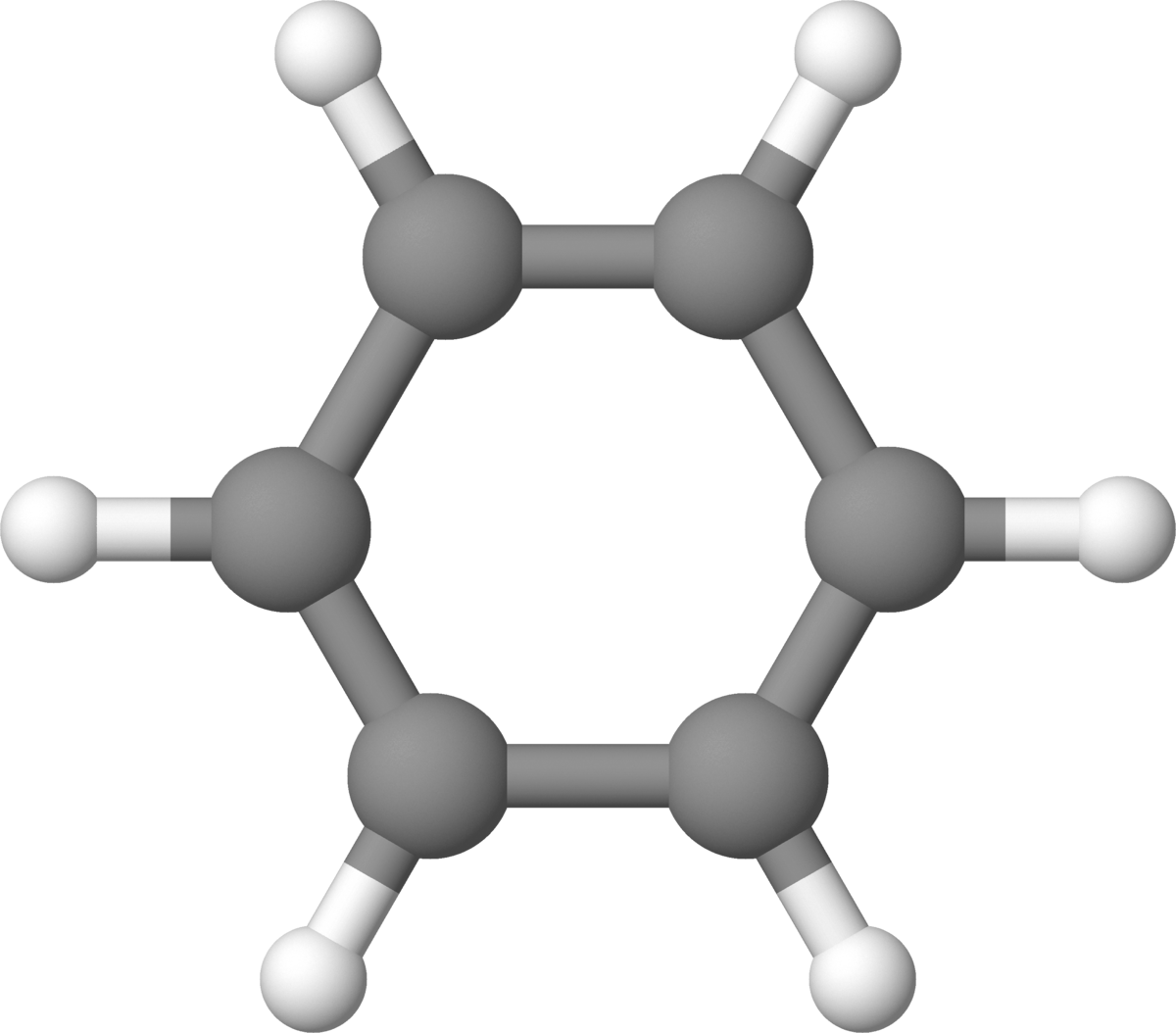
Aromatiske hydrokarboner inneholder en eller flere benzenringer. Navngiving av hydrokarboner følger visse konvensjoner, men i mange tilfeller, kan forbindelsene bli bedre kjent under eldre navn.
I moderne system, den første del av navnet representerer antallet karbonatomer i molekylet: i stigende rekkefølge, blir den første åtte prefiks met, etnisk, prop, knap, pent, heksa, hept- og Oct. Forbindelser der karboner er alle sluttet med enkeltbindinger er kjent kollektivt som alkaner,og har navn som slutter på -ane.
Molekyler som har dobbeltbindinger er kjent som alkener, og har navn som slutter på -en, mens de som har trippelbindinger kalles alkyner, og har navn som slutter på -yne. Karbonatomer kan også danne dobbel eller trippelbindinger med hverandre. Molekyler som har bare enkeltbindinger inneholder den maksimalt mulige antall hydrogenatomer, og er derfor beskrevet som mettet. Hvor det er dobbelt eller trippelbindinger, det er færre plasser tilgjeng.
See full list on notmywar. Mest produksjon av hydrokarboner er fra fossile brensler: kull, olje og naturgass, som er hentet fra bakken i mengder av millioner av tonn per dag. Råolje er for det meste en blanding av mange forskjellige alkaner og cykloalkaner, med noen aromatiske forbindelser.
Disse kan skilles fra hverandre ved oljeraffinerier ved destillering, på grunn av deres forskjellige kokepunkter. En annen fremgangsmåte som benyttes er kjent som "cracking": katalysatorer anvendes for å bryte noen av de større molekyler til mindre de som er mer nyttig som brensel.
Generelt sett, jo mer komplekst et hydrokarbon er, jo høyere smelte og kokepunkter. For eksempel, de enklere typer, slik som metan, etan og propan, med en, to og tre karbonatomer, henholdsvis er gasser. Mange former er væsker: eksempler er heksan og oktan.
De mest bemerkelsesverdige kjemiske egenskapene til hydrokarboner er deres brennbarhet og deres evne til å danne polymerer. De som er gasser eller væsker vil reagere med oksygen i luften, som produserer karbondioksyd (CO 2) og vann, og frigjøring av energi i form av lys og varme.
Litt energi må tilføres for å starte reaksjonen, men en gang startet, er det selvdrevet: disse forbindelsene vil brenne, som illustrert ved å tenne en gasskomfyr med en kamp eller gnist. I noen tilfeller vil ikke alt kar. Faste former vil også brenne, men mindre lett. Brennbarhet av hydrokarboner gjør dem svært nyttig som brensel, og de er den primære energikilden for dagens sivilisasjon.
På verdensbasis er mest elektrisitet generert ved forbrenning av disse forbindelsene, og de brukes til å drive praktisk talt alle mobil maskin: biler, lastebiler, tog, fly og skip. De kan også brukes ved fremstilling av mange andre kjemikalier og materialer. De fleste plastmaterialer, for eksempel, er hydrokarbonpolymerer. Andre bruksområder inkluderer løsemidler, smøremidler og drivmiddel for spraybokser.
Deres forbrenning produserer røyk og sot, forårsaker alvorlige forurensningsproblemer i enkelte områder. Den produserer også store mengder CO 2. Det er bred enighet blant forskere at økende nivåer av denne gassen i atmosfæren bidrar til å felle varme, heve globale temperaturer og skiftende jordens klima.
I tillegg vil fossilt brensel ikke vare evig. Brennende drivstoff på dagens rente, kunne oljen renne ut i mindre enn et århundre og kull i flere århundrer. Alt dette har ført til samtaler for å utvikle fornybare energikilder som sol- og vindkraft, og bygging av flere atomkraftverk, som produserer null CO 2-utslipp.
Opprinnelig gjaldt denne betegnelsen forbindelser som var avledet fra et stoff som heter benzen. Benzen har ei søtlig lukt, og derfor ble forbindelsen omtalt som aromatisk. I dag brukes betegnelsen om alle hydrokarboner med ringformede strukturer. Normal-alkaner (kjedeformede molekyler) finnes i størst mengde, man antar at alle n-alkaner med 1–karbonatomer finnes i råolje.
Behov for synonymer til HYDROKARBON for å løse et kryssord? Vi har også synonym til stoff og kjemisk stoff. Hydrokarbon har treff. Dette er en rapport fra forsøk 9. Egenskaper til hydrokarboner, fra læreboken "Kjemien Stemmer 1".
I dette forsøket skulle man studere et alkan, et alken og et aromatisk hydrokarbon og se hvordan de brenner og reagerer med brom, Br. Man skulle også se på løseligheten av disse hydrokarbonene i hverandre, i vann og i etanol.
Alkan er hydrokarbon med enkeltbindingar mellom alle atom. I alken er det dobbeltbinding mellom to karbonatom, og i alkyn er det trippelbinding.
Når karbonatomene danner lange kjeder, er det ofte i lag med andre grunnstoffer. Det er karbonatomene som danner grunnstrukturen (skjelettet) i hydrokarboner, de kan danne korte og lange kjeder.
Slike organiske forbindelser kalles hydrokarboner. Alifatiske hydrokarboner kan være mer eller mindre tyntflytende, og stoffene med lavest viskositet utgjør ofte det største problemet ved akutte perorale inntak. Tyntflytende alifatiske hydrokarboner kommer lett over i luftveiene ved svelging. Her spres væsken raskt og løser opp de overflateaktive stoffene i lungene.

Rapporten kommer inn på polære og upolære forbindelser. At dette kontinentet skal produsere energi til et velstående Europa – som ser på hydrokarboner som djevelens energi, mens Afrikas befolkning selv skriker etter elektrisitet, er absurd.
Petroleum består av hydrokarboner i ulike størrelser. Avhengig av størrelsen får hydrokarbonene forskjellige bruksområder. Derfor skiller vi disse etter størrelse når vi raffinerer oljen.
Naturgass består av de letteste hydrokarbonene, og inneholder for det meste metangass. LNG er navnet på naturgass når den har blitt kondensert til. Noe som er ganske interessant er hva som skjer hvis et hydrokarbon får satt på seg en polar gruppe, for eksempel -OH eller -COO.
Av LMProcrastinator, 4. Skole og leksehjelp.